Krivka topenia
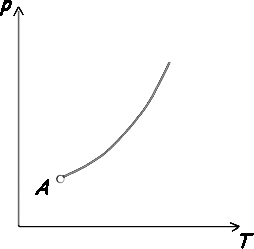
Na obrázku 1 je táto krivka
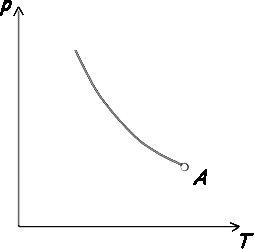
znázornená pre tuhé látky typu olovo, na obrázku 2 pre látku typu ľad H2O.
Každý bod tejto krivky znázorňuje rovnovážny stav tuhej a kvapalnej fázy
istej látky. Krivka topenia začína v bode A,
ktorému zodpovedá najmenší možný tlak, pri ktorom sú ešte kvapalina
a látka v rovnováhe.
1 2
Teploty topenia rôznych látok závisia od tlaku, udávajú
sa v tabuľkách pri normálnom tlaku a nazývajú sa normálne teploty topenia.
Látky,
pri ktorých sa so zvyšujúcim tlakom zvyšuje teplota topenia, svoj objem pri
topení zväčšujú a pri tuhnutí zmenšujú. Látky, ktoré pri zvýšení tlaku
svoju teplotu topenia znižujú, svoj objem pri topení zmenšujú a pri
tuhnutí zväčšujú.
Napr. pri ľade táto vlastnosť vyplýva z jeho kryštalickej štruktúry. Kryštálová mriežka je pretkaná priestorovými kanálikmi. Pri topení sa mriežka búra a voľný priestor sa zapĺňa molekulami vody. Zväčšenie objemu pri tuhnutí vody má veľký význam. Ľad má menšiu hustotu ako voda, preto na vode pláva a svojou nízkou tepelnou vodivosťou zabraňuje zamŕzaniu vody do väčšej hĺbky.