Krivka nasýtenej pary
Každý
bod krivky nasýtenej pary zodpovedá jednému stavu nasýtenej pary a súčasne
kvapaliny, ktorá je s ňou v rovnovážnom stave (dynamickej rovnováhe).
Tento stav je určený teplotou T a tlakom p. Množina týchto
bodov krivky nasýtenej pary znázorňuje teda všetky stavy rovnovážnej sústavy
kvapalina + nasýtená para.
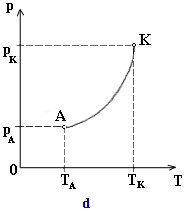
Začiatočnému
bodu A krivky (obr. d) prislúcha najmenšia hodnota teploty TA
a tlaku pA, pri ktorých existuje kvapalina
a nasýtená para v rovnovážnom stave. Teplota TA je
teplotou tuhnutia kvapalnej fázy pri tlaku pA (bodom A sa začína krivka topenia a končí sa
sublimačná).
Pri
zvyšovaní teploty rovnovážnej sústavy
kvapalina + nasýtená para stúpa hustota nasýtenej pary, hustota
kvapaliny naopak klesá. Rozhranie medzi kvapalinou a jej nasýtenou parou
je však stále ostré a zreteľné. Pri teplote TK, kritickej
teplote, sa hustota kvapaliny rovná hustote pary. Medzi kvapalinou
a jej nasýtenou parou zmizne rozhranie a látka sa stane rovnorodou.
Pri teplote vyššej ako TK už neexistuje látka
v kvapalnej fáze. Preto sa krivka nasýtenej pary končí v bode K (obr. d).
Koncový
bod krivky nasýtenej pary sa volá kritický bod a znázorňuje
kritický stav látky. Kritický stav je určený kritickou teplotou
TK kritickým tlakom pK a hustotou
Q . Veličiny TK , pK , ρK , sú
pre každú látku charakterizujúcimi konštantami.
Z krivky nasýtenej pary
príslušnej látky možno získať ešte jednu dôležitú informáciu a to teplotu
varu kvapaliny pri danom vonkajšom tlaku nad kvapalinou. Prečo je to tak, sa dá
vysvetliť rozborom varu z hľadiska molekulovej fyziky.
Pri vare sa vnútri kvapaliny
tvoria bubliny nasýtenej pary, ktoré zväčšujú svoj objem a vystupujú na
voľný povrch kvapaliny. Tento dej nastáva práve vtedy, keď tlak nasýtenej pary
bublín sa rovná približne vonkajšiemu tlaku. Keď sa zväčší tlak nad voľným
povrchom kvapaliny, var nastane až po takom zvýšení teploty kvapaliny, že sa
tlak vnútri bublín vyrovná vonkajšiemu tlaku. Teplota varu sa teda zvyšuje so
zvyšovaním vonkajšieho tlaku. Túto teplotu pre daný vonkajší tlak po
zistíme z krivky nasýtenej pary tak, že k tlaku nasýtenej pary ps
≐ po
vyhľadáme príslušnú teplotu.