Sublimácia
Premena látky z pevného
skupenstva priamo na plynné skupenstvo sa volá
sublimácia. Opačný dej je desublimácia.
Pri normálnom tlaku sublimuje napr. jód, gáfor, naftalín, tuhý oxid uhličitý,
ľad.
Merné
skupenské teplo sublimácie ls
, je definované vzťahom:
![]()
Kde Ls je
skupenské teplo sublimácie prijaté látkou s hmotnosťou m na jej
sublimáciu pri danej teplote. Merné skupenské teplo sublimácie závisí od
teploty, pri ktorej látka sublimuje.
Keď je sublimujúca látka s dostatočnou hmotnosťou
v uzavretej nádobe, sublimuje tak dlho, až sa medzi pevnou fázou
a parou utvorí rovnovážny stav. Vzniknutá para sa nazýva nasýtená para. Keď je teplota konštantná, pomer
hmotnosti plynného a pevného skupenstva zostáva konštantný a tlak
nasýtenej pary vzniknutý sublimáciou sa nemení.
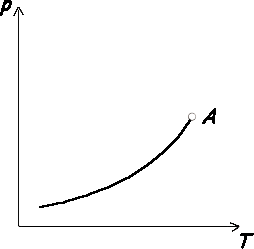
Závislosť tlaku nasýtenej pary
od teploty vyjadruje sublimačná krivka. Každý
bod tejto krivky súčastne znázorňuje rovnovážne stavy medzi pevnou látkou
a jej nesýtenou parou. Sublimačná krivka končí v bode A, v ktorom sa začína krivka topenia
tej istej látky